HOME > Information > アイモビーグ(片頭痛発作の発症抑制) | 名古屋~春日井の脳神経外科 | 勝川脳神経クリニック
アイモビーグ(片頭痛発作の発症抑制)
2021年6月23日承認
2021年8月12日発売
初回投与時も継続投与時も1回70㎎(1本)の投与(皮下注)/継続は4週に1回
経緯
アイモビーグ皮下注 70mg ペン」は,2018年、世界で最初に発売された CGRP 製剤です。
治療開始時、再開時においても 4 週間に 1 回 1 本皮下注射し、CGRP 製剤の中でも違った作用を持つ製剤です。
機序
片頭痛の原因とされる CGRP(カルシトニン関連ペプチド)は発作時に多く発現します。
CGRP を必要な分だけ取り込むため、受容体(受け皿)に蓋をすることで片頭痛の発作を抑える製剤です。
使用
お薬を始める時、また再開する時も 4 週間に 1 回 1 本を当院にて注射致します。
効果
①片頭痛の発作回数の減少。(※1)
②発作時の内服薬を減少。(※1)
③片頭痛による痛み、日常生活への影響が軽減。(※2)
日常生活での期待
片頭痛の発作を減らし、家事、仕事、学校での生活を快適にすることを期待します。
アイモビーグの特徴
①5年の長期投与試験により安全性が確認(※3)
②片頭痛患者様における64週後の片頭痛日数50%減少率は64.8%
③一度のご来院で1部位1本の注射で治療を行いますので、注射回数が少なくてすみます。(※4)
④抗体製剤の中でもアレルギー反応や効果が減弱することが少ないと言われる「完全ヒト化」の薬剤です。
(※1)こちらの結果は1ヶ月間の頭痛日数が15日未満でそのうち片頭痛日数が4日以上、または1ヶ月間の頭痛日数が15日以上でそのうち片頭痛日数が8日以上の方が対象となっています。
(※2)海外での成績
(※3)主な副作用として、注射部位のかゆみや赤み、便秘の報告
(※4)注射針カバーに乾燥天然ゴムを使用しておりますので、アレルギー症状あるの方はご相談ください。
アイモビーグの投与方法
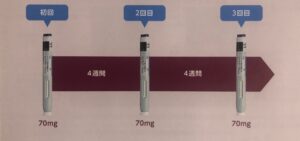
アイモビーグ®︎は、初めて投与する時から継続時、さらには中断後の再開時にも、4週間に1回1本と同じ用法用量で治療を行います。
・アイモビーグ®︎は、通常、成人にはエレヌマブ(遺伝子組換え)として70mgを4週間に1回皮下投与します。
・初回導入時も継続投与時も一貫して、1回の投与量は70mg(1本)です。
・患者の状態に応じて投与中断をご検討いただけます。なお、投与再開時の1回の投与量は70mg(1本)です。
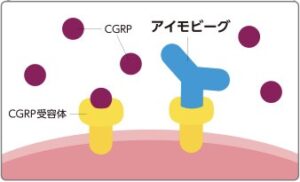
アイモビーグの作用機序
片頭痛の原因とされる CGRP(カルシトニン関連ペプチド)は発作時に多く発現することがわかっています。そのCGRP を必要な分だけ取り込むため、受容体(受け皿)に蓋をすることで片頭痛の発作を抑える製剤です。
カルシトニン遺伝子関連ペプチド(CGRP)は三叉神経の末端から放出され、血管周囲の神経原性炎症、血管の拡張、神経の興奮を惹起することにより、片頭痛発作の一因となると考えられています。アイモビーグ®︎はCGRPの受容体に選択的かつ高い親和性で結合することで作用を発揮します。
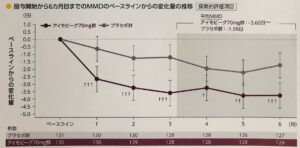
アイモビーグの効果①
アイモビーグ®︎は投与1ヶ月目から月間の片頭痛日数の減少が認められています。
アイモビーグ®︎70mg群はプラセボ群と比較して投与1ヶ月目から有意差をもってMMD(平均月間片頭痛日数)の減少が認められ、その作用は6ヶ月目まで維持しました。
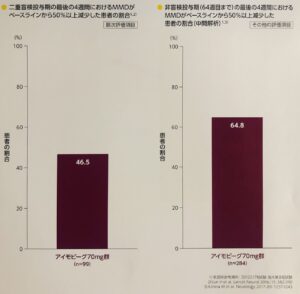
アイモビーグの効果②
アイモビーグ®︎で治療を行った患者さんにおいて、治療開始3ヶ月後に46.5%、一年経過後に64.5%の患者さんで月間の片頭痛日数が50%減少したことが認められています。
反復性片頭痛患者を対象とした海外第Ⅱ相試験では、アイモビーグ®︎70mgを投与した患者におけるMMD(平均月間片頭痛日数)がベースラインから50%以上減少した患者の割合は、二重盲検投与期の最後の4週間において46.5%、非盲検投与期(64週目まで)の最後の4週間において64.8%でした。
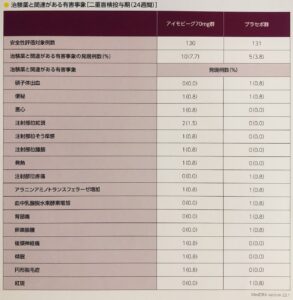
アイモビーグの有害事象
アイモビーグ®︎と関連がある副作用は7.7%(130例中10例)で、主なものとして、注射部位の赤み、便秘などが報告されています。
日本人片頭痛患者を対象とした国内第三相試験では二重盲検投与期(24週間)において、治験薬と関連がある有害事象の発現割合はアイモビーグ®︎70mg群で7.7%、プラセボ群で3.8%でした。主なものは、注射部位紅斑(2例)でした。
ヒト抗CGRP受容体モノクローナル抗体製剤『アイモビーグ』
1.禁忌
本剤の成分に対し過敏症の既往歴のある患者
2.本剤の組成
販売名 アイモビーグ皮下注70mgペン(1mlの分量)
有効成分 エレヌマブ(遺伝子組換え) 70mg
添加剤 精製白糖 73mg
ポリソルベート80 0.1mg
pH調整剤 適量
注)遺伝子組換え技術によりチャイニーズハムスター卵巣細胞を用いて製造
3.効能又は効果
片頭痛発作の発症抑制
4.効能又は効果に関連する注意
①十分な診察を実施し、前兆のある又は前兆のない片頭痛の発作が月に複数回以上発現している、又は慢性片頭痛であることを確認した上で本剤の適用を考慮すること。
②最新のガイドライン等を参考に、非薬物療法、片頭痛発作の急性期治療等を適切に行っても日常生活に支障をきたしている患者にのみ投与すること。
①-1慢性頭痛の診療ガイドライン2013(慢性頭痛の診療ガイドライン作成委員会, 2013)において、
片頭痛が月に2回以上あるいは6日以上あるような患者では予防療法の実施について検討することが勧められていることを踏まえて設定しました。
②-1予防療法の適応となるのは片頭痛発作の急性期治療のみでは日常生活に支障をきたしている患者である旨記載されていることを踏まえて設定しました。
5.重要な基本的情報
①本剤は片頭痛の治療に関する十分な知識及び経験を有する医師のもとで使用すること。
②本剤は発現した頭痛発作を緩解する薬剤ではないので、本剤投与中に頭痛発作が発現した場合には必要に応じて頭痛発作治療薬を頓用させること。投与前にこのことを患者に十分に説明しておくこと。
③本剤投与後に、重篤な合併症を伴う便秘が発現する場合があることを患者に説明し、便秘が回復しない又は悪化する場合には医療機関を受診するよう患者に指導する こと。特に、便秘の既往歴を有する患者及び消化管運動低下を伴う薬剤を併用して いる患者では発現リスクが高くなるおそれがあるため注意すること。
④本剤の注射針カバーは天然ゴム(ラテックス)を含み、アレルギー反応を起こすことがあるので、投与に際し、問診を行うこと。